Aldehído

Los aldehídos son compuestos orgánicos caracterizados por poseer el grupo funcional -CHO (carbonilo).[1] Un grupo carbonilo es el que se obtiene separando un átomo de hidrógeno del formaldehído. Como tal no tiene existencia libre, aunque puede considerarse que todos los aldehídos poseen un grupo terminal carbonilo.
Los aldehídos se denominan como los alcoholes correspondientes, cambiando la terminación -ol por -al.[2] Etimológicamente, la palabra aldehído proviene del latín científico alcohol dehydrogarium (alcohol deshidrogenado).[3]
Estructura y enlace[editar]
Los aldehídos presentan un carbono central que está unido por un doble enlace al oxígeno y un enlace sencillo al hidrógeno y un enlace sencillo a un tercer sustituyente, que es el carbono o, en el caso del formaldehído, el hidrógeno. El carbono central suele describirse como sp2-hibridado. El grupo aldehído es algo polar. La longitud de enlace C=O es de unos 120-122 picómetros.[4]
Propiedades[editar]
Propiedades Físicas[editar]
- La doble unión del grupo carbonilo se debe a que el grupo carbonilo está polarizado[5] debido al fenómeno de resonancia.
- Los aldehídos con hidrógeno sobre un carbono sp³ en posición alfa al grupo carbonilo presentan isomería tautomérica. Los aldehídos se obtienen de la deshidratación de un alcohol primario con permanganato de potasio, la reacción tiene que ser débil, las cetonas también se obtienen de la deshidratación de un alcohol, pero estas se obtienen de un alcohol secundario e igualmente son deshidratados con permanganato de potasio y se obtienen con una reacción débil, si la reacción del alcohol es fuerte, el resultado será un ácido carboxílico respectivamente.
Los aldehídos tienen propiedades diversas que dependen del resto de la molécula. Los aldehídos más pequeños son más solubles en agua, formaldehído y acetaldehído completamente. Los aldehídos volátiles tienen olores penetrantes.
Los aldehídos pueden identificarse por métodos espectroscópicos. Mediante espectroscopia IR, muestran una banda CO fuerte cerca de 1700 cm-1. En sus espectros de 1H NMR, el centro de hidrógeno del formilo absorbe cerca de δH 9,5 a 10, que es una parte distintiva del espectro. Esta señal muestra el acoplamiento característico a cualquier protón del carbono α con una pequeña constante de acoplamiento típicamente inferior a 3,0 Hz. Los espectros 13C NMR de aldehídos y cetonas dan una señal suprimida (débil) pero distintiva en C 190 a 205.
Propiedades Químicas[editar]
- Se comportan como reductor, por oxidación el aldehído da ácidos con igual número de átomos de carbono.
- La reacción típica de los aldehídos y las cetonas es la adición nucleofílica.
Aplicaciones y aparición[editar]
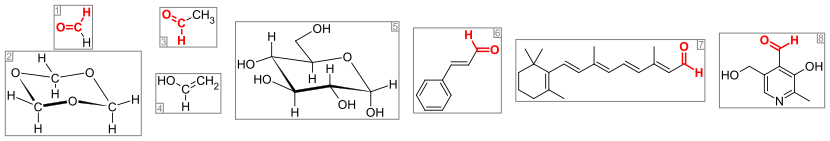
Aldehídos importantes y compuestos relacionados. El grupo aldehído (o grupo formilo) está coloreado en rojo. Desde la izquierda: (1) formaldehído y (2) su trímero 1,3,5-trioxano, (3) acetaldehído y (4) su enol alcohol vinílico, (5) glucosa (forma piranosa como α-D-glucopiranosa), (6) el saborizante cinamaldehído, (7) retinal, que se forma con opsinas fotorreceptores, y (8) la vitamina piridoxal.
Aldehídos naturales[editar]
En los aceites esenciales se encuentran trazas de muchos aldehídos que a menudo contribuyen a sus olores favorables, por ejemplo, cinamaldehído, cilantro y vainillina. Posiblemente debido a la alta reactividad del grupo formilo, los aldehídos no son comunes en varios de los bloques de construcción naturales: aminoácidos, ácidos nucleicos, lípidos. Sin embargo, la mayoría de los azúcares son derivados de aldehídos. Estas aldosas existen como hemiacetales, una especie de forma enmascarada del aldehído original. Por ejemplo, en solución acuosa sólo una pequeña fracción de la glucosa existe como aldehído.
Nomenclatura[editar]
Se nombran sustituyendo la terminación -ol del nombre del alcohol por -al. Los aldehídos más simples (metanal y etanal) tienen otros nombres que no siguen el estándar de la Unión Internacional de Química Pura y Aplicada (IUPAC) pero son más utilizados formaldehído y acetaldehído, respectivamente, estos últimos dos son nombres triviales aceptados por la IUPAC. La serie homóloga para los siguientes aldehídos es: H-(CH
2)
n-CHO (n = 0, 1, 2, 3, 4, …)
| Número de carbonos | Nomenclatura IUPAC | Nomenclatura trivial | Fórmula | P.E.°C |
|---|---|---|---|---|
| 1 | Metanal | Formaldehído | HCHO | -21 |
| 2 | Etanal | Acetaldehído | CH 3CHO |
20,2 |
| 3 | Propanal | Propionaldehído Propilaldehído |
C 2H 5CHO |
48,8 |
| 4 | Butanal | n-Butiraldehído | C 3H 7CHO |
75,7 |
| 5 | Pentanal | n-Valeraldehído Amilaldehído n-Pentaldehído |
C 4H 9CHO |
103 |
| 6 | Hexanal | Capronaldehído n-Hexaldehído |
C 5H 11CHO |
100.2 |
| 7 | Heptanal | Enantaldehído Heptilaldehído n-Heptaldehído |
C 6H 13CHO |
48.3 |
| 8 | Octanal | Caprilaldehído n-Octilaldehído |
C 7H 15CHO |
Entre 55.381 y 55.389 (Aproximadamente) |
| 9 | Nonanal | Pelargonaldehído n-Nonilaldehído |
C 8H 17CHO |
62.47 |
| 10 | Decanal | Caprinaldehído n-Decilaldehído |
C 9H 19CHO |
10.2 |
Para nombrar aldehídos como sustituyentes

Si es sustituyente de un sustituyente

Los aldehídos son funciones terminales, es decir que van al final de las cadenas Nomenclatura de ciclos
| Localizador | Cadena Carbonada Principal | Carbaldehido | Ejemplo |
|---|---|---|---|
| 1(se puede omitir) | Benceno | Carbaldehido | 
|
| 2,3 | Naftaleno | DiCarbaldehido | 
|
Si el ciclo presenta otros sustituyentes menos importantes se los nombre primeros, así:
Para mayores detalles consulte Nomenclatura de aldehídos
Reacciones de los aldehídos[editar]
Los aldehídos aromáticos como el benzaldehído se dismutan en presencia de una base dando el alcohol y el ácido carboxílico correspondiente:
2 C
6H
5CHO → C
6H
5CH
2OH + C
6H
5CO
2H
Con aminas primarias dan las iminas correspondiente en una reacción exotérmica que a menudo es espontánea:
R-CH=O + H
2N-R' → R-CH=N-R'
En presencia de sustancias reductoras como algunos hidruros o incluso otros aldehídos pueden ser reducidos al alcohol correspondiente mientras que oxidantes fuertes los transforman en el correspondiente ácido carboxílico.
Con cetonas que portan un hidrógeno sobre un carbono sp³ en presencia de catalizadores ácidos o básicos se producen condensaciones tipo aldol.
Con alcoholes o tioles en presencia de sustancias higroscópicas se pueden obtener acetales por condensación. Como la reacción es reversible y los aldehídos se recuperan en medio ácido y presencia de agua esta reacción se utiliza para la protección del grupo funcional.
Síntesis[editar]

Existen varios métodos para preparar aldehídos, pero la tecnología dominante es la hidroformilación.[6] Ilustrativa es la generación de butiraldehído por hidroformilación de propeno:
- Por oxidación de alcoholes primarios
Se pueden obtener a partir de la oxidación suave de los alcoholes primarios. Esto se puede llevar a cabo calentando el alcohol en una disolución ácida de dicromato de potasio (también hay otros métodos en los que se emplea Cr en el estado de oxidación +6). El dicromato se reduce a Cr3+
(de color verde). También mediante la oxidación de Swern, en la que se emplea dimetilsulfóxido, (DMSO), dicloruro de oxalilo, (CO)
2Cl
2, y una base. Esquemáticamente el proceso de oxidación es el siguiente:[7]
- Por carbonilación.
- Por oxidación de halogenuros de alquilo (Oxidación de Kornblum)
- Por reducción de ácidos carboxílicos o sus derivados (ésteres, halogenuros de alquilo).
Rutas oxidativas[editar]
Los aldehídos se generan comúnmente por oxidación de alcoholes. En la industria, el formaldehído se produce a gran escala por oxidación del metanol.[8] El oxígeno es el reactivo de elección, por ser "verde" y barato. En el laboratorio, se utilizan agentes oxidantes más especializados, pero los reactivos de cromo(VI) son muy populares. La oxidación puede conseguirse calentando el alcohol con una solución acidificada de dicromato potásico. En este caso, el exceso de dicromato oxidará aún más el aldehído a un ácido carboxílico, por lo que o bien el aldehído es destilado tal como se forma (si volátil) o se utilizan reactivos más suaves como el PCC.[7]
La oxidación de alcoholes primarios para formar aldehídos puede lograrse en condiciones más suaves y sin cromo empleando métodos o reactivos como ácido IBX, periodinano de Dess-Martin, oxidación de Swern, TEMPO o la oxidación de Oppenauer.
Otra ruta de oxidación significativa en la industria es el proceso Wacker, por el que el etileno se oxida a acetaldehído en presencia de catalizadores de cobre y paladio (el acetaldehído también se produce a gran escala por hidratación del acetileno).
A escala de laboratorio, los α-hidroxiácidos se utilizan como precursores para preparar aldehídos mediante escisión por oxidativa.[9][10]
Síntesis de aldehídos aromáticos[editar]
- Reacción de Gattermann-Koch
- Reacción de Hoesch
- Reacción de Reimer-Tiemann
- Reacción de Vilsmeier-Haack
Métodos de especialidad[editar]
| Nombre de la reacción | Substrato | Comentarios |
|---|---|---|
| Ozonólisis | Alquenos | La ozonólisis de alquenos no totalmente sustituidos da lugar a aldehídos tras una elaboración reductora. |
| Reducción orgánica | Ésteres | Reducción de un éster con hidruro de diisobutilaluminio (DIBAL-H) o hidruro de aluminio y sodio. |
| Reacción de Rosenmund | Cloruro de acilo | Cloruros de acilo selectivamente reducidos a aldehídos. El hidruro de litio tri-t-butoxialuminio (LiAlH(Ot Bu) 3) es un reactivo eficaz.[cita requerida] |
| Reacción de Wittig | Cetonas | Una reacción de Wittig modificada utilizando metoximetilentrifenilfosfina como reactivo. |
| Reacción de formilación | Nucleófilo arenos | Diversas reacciones, por ejemplo la reacción de Vilsmeier-Haack. |
| Reacción de Nef | Nitrocompuestos | La ácido hidrólisis de un primario para formar un aldehído. |
| oxidación de Kornblum | Haloalcanos | La oxidación de un haluro primario con dimetilsulfóxido para formar un aldehído. |
| Reacción de Zincke | Piridinas | |
| Síntesis del aldehído de Stephen | Nitrilos | Hidrólisis de una sal de iminio generada por cloruro de estaño(II) y HCl para formar un aldehído. |
| Hidrólisis de halogenuro de gemina | Geminal dihaluros | Hidrólisis de primarios dihaluros gemínicos para producir aldehídos. |
| Síntesis de Meyers | Oxazinas | Hemiaminal hidrólisis de oxazina con agua y ácido oxálico para producir un aldehído. |
| Variación de la Transposición de Hofmann[11][12] | insaturados o α-hidroxi amidas | Aldehídos mediante la hidrólisis de un intermedio carbamato. |
| Reacción de McFadyen-Stevens | Hidrazidas | Base-catalizada Descomposición térmica de acilsulfonilhidrazidas. |
| Biotransformación | Alquenos | Liofilizados cultivos celulares de Trametes hirsuta en presencia de oxígeno.[13] |
Usos[editar]
Los aldehídos se utilizan principalmente para la fabricación de resinas, plásticos, solventes, pinturas, perfumes, esencias.
Los aldehídos están presentes en numerosos productos naturales y grandes variedades de ellos son de la propia vida cotidiana. La glucosa por ejemplo existe en una forma abierta que presenta un grupo aldehído. El acetaldehído formado como intermedio en la metabolización se cree responsable en gran medida de los síntomas de la resaca tras la ingesta de bebidas alcohólicas.
El formaldehído es un conservante que se encuentra en algunas composiciones de productos cosméticos. Sin embargo esta aplicación debe ser vista con cautela ya que en experimentos con animales el compuesto ha demostrado un poder cancerígeno. También se utiliza en la fabricación de numerosos compuestos químicos como la baquelita, la melamina, etc.
Referencias[editar]
- ↑ Diccionario de ciencias. Editorial Complutense. 2000. ISBN 9788489784802. Consultado el 18 de noviembre de 2017.
- ↑ Química 2 (SEP). Ediciones Umbral. ISBN 9789685607513. Consultado el 18 de noviembre de 2017.
- ↑ Real Academia Española. «aldehído». Diccionario de la lengua española (23.ª edición). Consultado el 23 de junio de 2012.
- ↑ G. Berthier, J. Serre (1966). «Aspectos generales y teóricos del grupo carbonilo». En Saul Patai, ed. El grupo carbonilo. PATAI'S Chemistry of Functional Groups 1. John Wiley & Sons. pp. 1-77. ISBN 9780470771051. doi:10.1002/9780470771051.ch1.
- ↑ Fieser, Louis F.; Fieser, Mary (1981). Química orgánica fundamental. Reverte. ISBN 9788429171617. Consultado el 18 de noviembre de 2017.
- ↑ Bertleff, W.; Roeper, M. y Sava, X. (2003) "Carbonylation" in Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH: Weinheim. doi 10.1002/14356007.a05_217.pub2
- ↑ a b Ratcliffe, R. W. (1988). "Oxidation with the Chromium Trioxide-Pyridine Complex Prepared in situ: 1-Decanal". Org. Synth.; Coll. Vol. 6: 373.
- ↑ Error en la cita: Etiqueta
<ref>no válida; no se ha definido el contenido de las referencias llamadasCH2O - ↑ Ōeda, Haruomi (1934). «Oxidation of some α-hydroxy-acids with lead tetraacetate». Bulletin of the Chemical Society of Japan 9 (1): 8-14.
- ↑ Nwaukwa, Stephen; Keehn, Philip (1982). «Oxidative cleavage of α-diols, α-diones, α-hydroxy-ketones and α-hydroxy- and α-keto acids with calcium hypochlorite [Ca(OCl)2]». Tetrahedron Letters 23 (31): 3135-3138.
- ↑ Weerman, R.A. (1913). «Einwirkung von Natriumhypochlorit auf Amide ungesättigter Säuren». Justus Liebigs Annalen der Chemie 401 (1): 1-20. doi:10.1002/jlac.19134010102.
- ↑ Everett, Wallis; Lane, John (1946). «The Hofmann Reaction». Organic Reactions 3 (7). pp. 267-306. ISBN 9780471005285. doi:10.1002/0471264180.or003.07.
- ↑ Sutton, Peter; Whittall, John (2012). Métodos prácticos para biocatálisis y biotransformaciones 2. Chichester, West Sussex: John Wiley & Sons, Ltd. pp. 199-202. ISBN 9781119991397.
Bibliografía[editar]
- PETERSON, W.R. Formulación y Nomenclatura Química Orgánica (6ta edición). Barcelona-España: Eunibar-editorial universitaria de Barcelona. pp. 98-101.


![{\displaystyle {\ce {[O] + CH3(CH2)9OH -> CH3(CH2)8CHO + H2O}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/4fe12103929f870bd0f268e0ff4023984be8707d)